お知らせ
- 2026.3.6 2026年3月倫理審査委員会議事録概要を掲載いたしました
- 2026.4.21 2026年3月治験審査委員会(IRB)議事録概要を掲載いたしました。
- 2026.3.18 「2026年度 治験審査委員会 開催日程」を掲載いたしました
- 2026.3.10 2026年2月治験審査委員会(IRB)議事録概要を掲載いたしました。
- 2025.10.30 2025年10月倫理審査委員会議事録概要を掲載いたしました
- 2025.10.10 「治験受託前の文書の保管について」を掲載いたしました
- 2025.8.26 重大な不適合報告の情報を公開いたしました
- 治験審査委員会:原則毎月第2水曜日開催
ごあいさつ
兵庫県のがん診療の中心的役割を担う当センターでは質の高いがん診療を行うとともに、将来のより良いがん治療の開発に取り組んでいます。将来の新規治療につながる臨床試験を数多く行うことで、患者さんが臨床試験を選ぶ機会を増やせます。臨床試験を受けることで、新しい治療が受けられ、治療選択肢が増えるチャンスになり、治療や検査の費用負担が軽くなる等のメリットがあります。反面、思い描く効果が得られないことや、副作用の可能性もあります。当課では、臨床試験の依頼者と密に連絡を取りより質の高い臨床試験を導入し、院内で適切、安全に臨床試験を行う体制を築くとともに、データを迅速に作成・報告するように努めております。臨床試験の参加を考慮される際にその理解を助け、希望にそう意思決定ができるよう、また試験を受けられている間にも不安なく、安全に検査や治療が受けられるように患者さんに寄り添い、院内各所の連携にもチーム一体となって取り組んでおります。
ゲノム医療・臨床試験センター長
里内 美弥子
概要
当センターは、がん専門病院として患者さんに最善の診療を行うことを心がけていますが、それだけでなくより優れた新しい診断や治療法の開発を行うことも大きな使命であると考えています。新しい診断や治療法(薬剤)を科学的に評価する方法が臨床試験です。新しい法律、新GCP(「医薬品の臨床試験の実施に関する基準」で求められている治験の質(倫理性、科学性、信頼性)を確保するため専任の臨床試験コーディネーター(CRC;Clinical Research Coordinator)が活動しています。 CRCは臨床試験に参加してくださる患者さんと医師の橋渡しとして、各部門のスタッフと連携をとり治験を安全にかつ円滑に実施しています。 具体的な業務内容としては、治験の説明や不安や疑問への対応、治験薬に関する情報提供、治験スケジュールの管理、治験に必要なデータ収集などです。事務部門は各委員会への申請書類の管理、申請者への対応をおこない、治験及び臨床試験をおこなう上での事務手続きに対応しています。
組織図
2024年5月1日現在
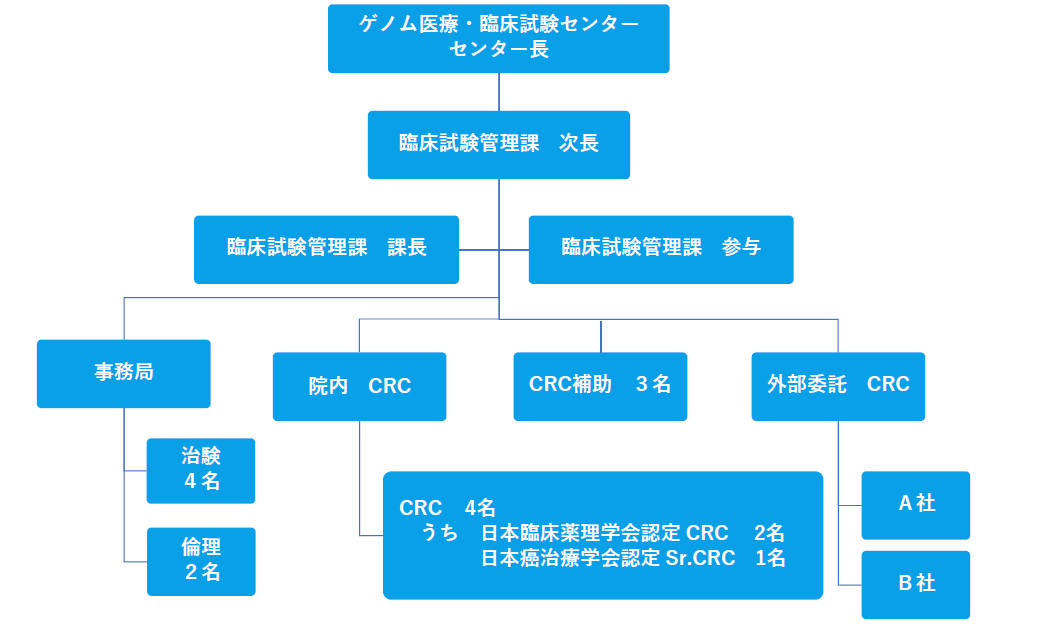
当院における治験実績
がんセンターで実施している治験は、兵庫県内外から患者の関心が集まり問い合わせや参加があります。実施数は、年間約90件を維持しており、第1相試験(新薬開発初期段階)の受託も年々増加しています。
年度別治験実施数